- HOME
- 東レAPOA2-iTQについて
- 製品情報
製品情報
重要な基本的注意
- 本品は類縁疾患でも陽性の結果となる場合があることから、本品の結果のみで膵癌の診断はできないことに留意すること。
- 早期膵癌の場合には、本品による検出ができない可能性があることに留意すること。
全般的な注意
- 本品は体外診断用医薬品であり、それ以外の目的に使用しないでください。
- 診断の際は、他の関連する検査結果や臨床情報などとあわせて医師が総合的に判断してください。
- 本電子添文に記載された使用方法に従って使用してください。本電子添文に記載された使用目的及び使用方法以外での使用については保証いたしません。
- 使用する機器の添付文書又は取扱説明書をよく読んでから使用してください。
製品概要
詳細は電子添文をご参照ください。また、電子添文の改訂にご留意ください。
(下記情報は2023年11月改訂(第2版)の電子添文に基づき作成)
使用目的
血漿又は血清中のアポリポ蛋白A2(APOA2)アイソフォームの測定(膵癌の診断の補助)
測定原理
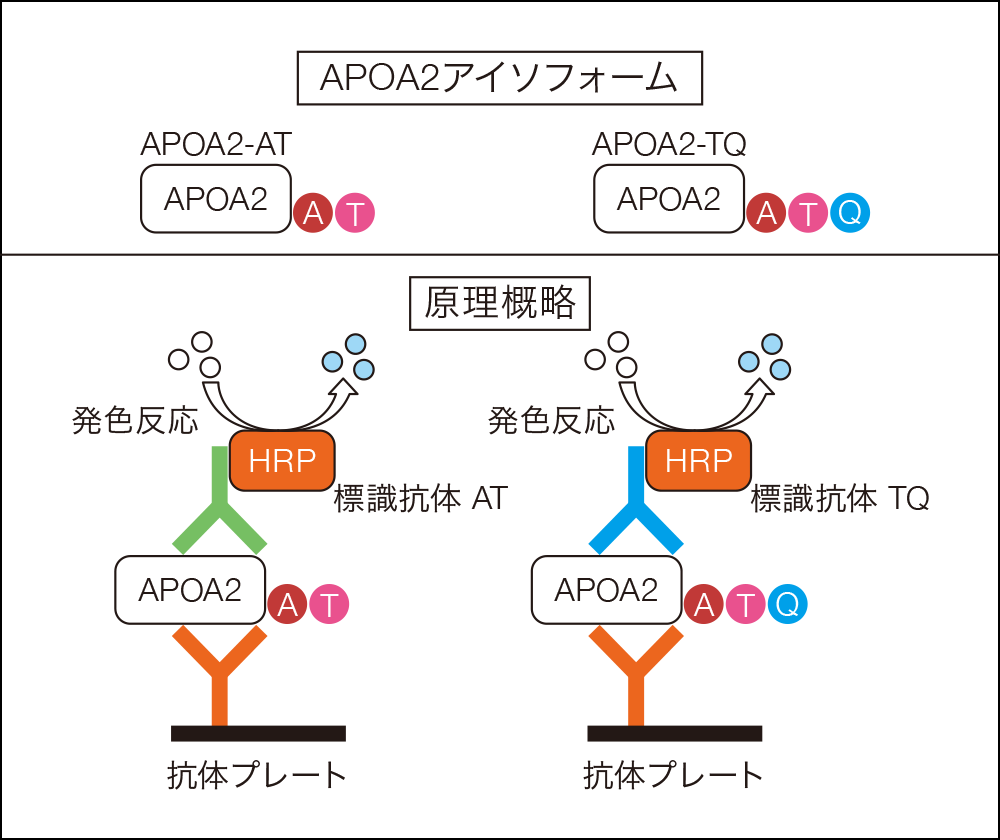
本品は、サンドイッチ法を原理とする酵素免疫測定法(ELISA)により、2種類のAPOA2アイソフォーム(APOA2-AT及びAPOA2-TQ)濃度を測定するキットです。
マウス抗APOA2非末端モノクローナル抗体が固相化されたウェルに検体を加えると、抗原であるAPOA2アイソフォーム量に応じて抗原-抗体複合体が形成されます。未反応の検体を洗浄除去後、酵素標識抗体を加えることで、抗体-抗原-酵素標識抗体の複合体を形成します。未反応の酵素標識抗体を洗浄除去後、基質を加えて発色反応を行い、反応停止後、吸光度を測定します。同時に測定した各種濃度の検量線用標準液の吸光度から作成した検量線を用いて、検体中の2種類のAPOA2アイソフォーム濃度を算出します。
形状・構造等(キットの構成)
- 抗体プレート(8ウェル×12ストリップ) 2枚(マウス抗APOA2非末端モノクローナル抗体)
- 標準液AT(20.8ng/mL) 1mL×1本
- 標準液TQ(36.8ng/mL) 1mL×1本
- 検体希釈液 100mL×2本
- 濃縮洗浄液 100mL×1本
- 標識抗体AT 0.25mL×1本(Horseradish peroxidase 標識ウサギ抗APOA2-AT ポリクローナル抗体)
- 標識抗体TQ 0.25mL×1本(Horseradish peroxidase 標識マウス抗APOA2-TQ モノクローナル抗体)
- 標識抗体希釈液 25mL×1本
- 基質液 25mL×1本(3,3’,5,5’-テトラメチルベンジジン)
- 停止液 25mL×1本
- プレートシール 6枚
(注)2, 3, 6, 7, 9 は遮光保存品。5は別売りも有り
貯蔵方法・有効期間
1. 貯蔵方法
凍結を避け、2~8°Cで保存してください。
2. 有効期間
製造後15ヶ月(包装に表示の使用期限内に使用してください。)
包装単位
96 テスト
関連情報
- 承 認 番 号:30500EZX00026000
- 製造販売承認年月:2023年6月
- 販売開始年月:2024年2月
使用方法
用法・用量(操作方法)
1. 試薬の調製方法
試薬は20~30°C(目安)に戻してから使用してください。
- 希釈検体
検体(血漿又は血清)は検体希釈液で10,000倍希釈して使用してください。希釈検体が不均一にならないよう、希釈時は十分に攪拌してください。
希釈した検体試料は即日測定してください。
例:検体10µL + 検体希釈液990µL → 100倍希釈検体
100倍希釈検体10µL + 検体希釈液990µL→ 10,000倍希釈検体 - 洗浄液
濃縮洗浄液を精製水で15倍希釈して使用してください。
濃縮洗浄液に析出物がある場合は、40°Cを目安に加温して溶解した後に使用してください。また、粘性が高いため、希釈時は十分に攪拌してください。
洗浄液は、25°C以下で28日間保存可能です。 - 検量線用標準液
標準液AT及び標準液TQを検体希釈液で2倍段階希釈して、各8濃度の検量線用標準液を調製して使用してください。
APOA2-AT:20.8, 10.4, 5.2, 2.6, 1.3, 0.65, 0.325, 0ng/mL
APOA2-TQ:36.8, 18.4, 9.2, 4.6, 2.3, 1.15, 0.575, 0ng/mL
(注)0ng/mLは検体希釈液をそのまま使用してください。 - 標識抗体液
標識抗体AT及び標識抗体TQを標識抗体希釈液で61倍希釈して使用してください。
標識抗体液は25°C以下で24時間保存可能です。 - その他試薬
そのまま使用してください。
2. 必要な器具・器材・試料等
- マイクロピペット
- マルチチャンネルピペット
- マイクロチューブ又はディープウェルプレート等
- メスシリンダー
- ペーパータオル
- インキュベータ(設定22~28°C)
- プレートウォッシャー
- マイクロプレート分光光度計(測定波長450~650nm)
- 精製水
3. 測定(操作)法
本品ではAPOA2-AT濃度及びAPOA2-TQ濃度を別々に測定します。
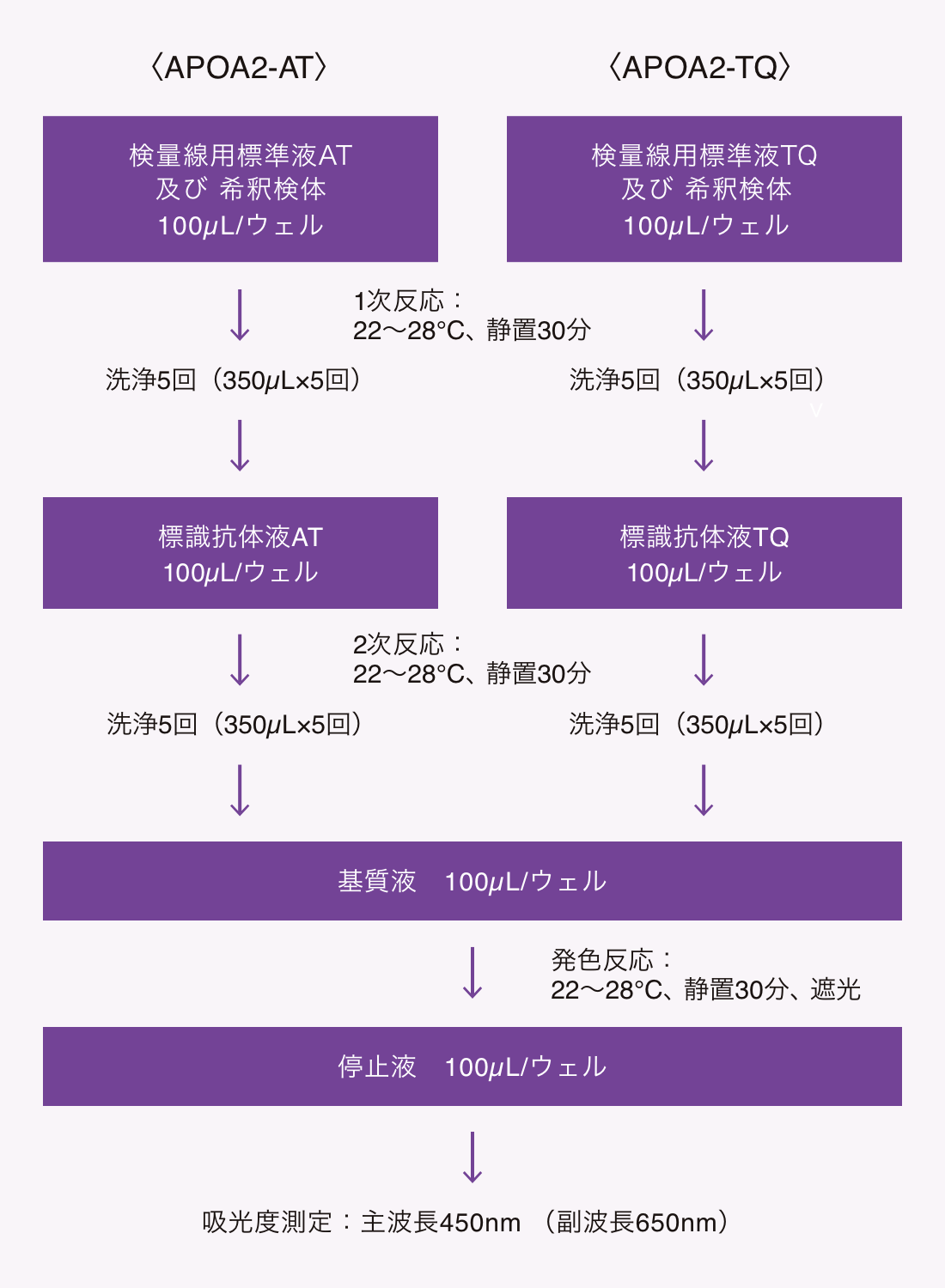
- 抗体プレート(以下、プレートと称す)の各ウェルに、検量線用標準液(二重測定)及び希釈検体を100µLずつ分注した後、プレートシールでカバーし、22~28°Cで30分間静置します(1次反応)。
- プレートシールをはがし、ウェル内の液を除去後、洗浄液を各ウェルに350µLずつ分注し、洗浄液を除去します。さらにこれを4回繰り返し、プレートをペーパータオル等の上に逆さに置き、洗浄液を十分に除去します。
- 標識抗体液を各ウェルに100µLずつ分注し、プレートシールでカバーし、22~28°Cで30分間静置します(2次反応)。
- ②と同じ操作でプレートを洗浄します。
- 基質液を各ウェルに100µLずつ分注し、プレートシールでカバーし、遮光して22~28°Cで30分間静置します(発色反応)。
- プレートシールをはがし、停止液を各ウェルに100µLずつ分注し、プレートを30秒間振盪します。
- 停止液を分注後30分以内に、マイクロプレート分光光度計を用いて、各ウェルの主波長450nm(副波長650nm)の吸光度を測定します。
- 横軸に各検量線用標準液の濃度(ng/mL)を、縦軸に吸光度の平均値をとり検量線を作成し、各希釈検体中のAPOA2-AT濃度及びAPOA2-TQ濃度を算出します。
- 算出濃度に希釈倍率(10,000)を乗じ、検体中のAPOA2-AT濃度及びAPOA2-TQ濃度(µg/mL)を算出します。
測定結果の判定法
検体中のAPOA2-AT濃度及びAPOA2-TQ濃度を算出し、APOA2-AT濃度とAPOA2-TQ濃度の相乗平均値(APOA2-i Index)をもとに判定します。
APOA2-i Index = √(APOA2-AT濃度×APOA2-TQ濃度)
ただし、検体中のAPOA2-AT濃度が3.25µg/mL未満又はAPOA2-TQ濃度が5.75µg/mL未満である場合は、APOA2-i Indexを0(ゼロ)µg/mL としてください。
1. 参考基準範囲1)
- 男性1,025例、女性975例の合計2,000例の健常人の血漿APOA2アイソフォーム濃度を測定した結果、以下のようになりました。
APOA2-i Index:健常人の95%が59.5µg/mL 以上(平均値:89.2µg/mL)
なお、このときのAPOA2-AT濃度とAPOA2-TQ濃度の範囲(最小値~最大値)は以下のようになりました。
APOA2-AT:6.11~197.58µg/mL
APOA2-TQ:19.18~279.49µg/mL - 基準範囲は種々の条件下、各施設により変動する可能性がありますので、各施設にて適した値を設定してください。
2. 判定上の注意
- 測定範囲の上限を超える高濃度検体については、測定範囲に入るよう検体希釈液で希釈倍率を調整してください。
- APOA2アイソフォームの膵癌に対する特異性は絶対的なものではなく、類縁疾患(慢性膵炎、IPMNなど)や他の消化器癌においてもAPOA2-i Index が低下する場合があるため、判定は注意してください。
臨床的意義(電子添文より抜粋)
5. 検体種間の相関性
同一検体の血漿と血清各50例について相関性を検討した結果、回帰式及び相関係数rは以下の通りとなりました。
APOA 2-AT:y=1.09x+ 0.99、r= 0.96
APOA 2-TQ:y= 0.90x+4.94 、r= 0.93
APOA 2-i Index:y= 0.94x+4. 34 、r= 0.91
(x:血漿、y:血清)
性能
1. 性能
- 感度
APOA2-ATについて、0ng/mL及び0.325ng/mLの標準液を3回測定するとき、0.325ng/mLの吸光度の平均値-2SDは0ng/mLの吸光度の平均値+2SD以上になります。
APOA2-TQについて、0ng/mL及び0.575ng/mLの標準液を3回測定するとき、0.575ng/mLの吸光度の平均値-2SDは0ng/mLの吸光度の平均値+2SD以上になります。 - 正確性
APOA2-AT及びAPOA2-TQそれぞれについて、既知濃度の管理検体を各濃度3回測定するとき、算出濃度は既知濃度の100±20%以内になります。 - 同時再現性
APOA2-AT及びAPOA2-TQそれぞれについて、既知濃度の管理検体を各濃度3回同時に測定するとき、算出濃度のCVはそれぞれ15%以下になります。
2. 測定範囲
APOA2-AT:0.325~20.8ng/mL
APOA2-TQ:0.575~36.8ng/mL
(注)希釈検体としての測定範囲です。
3. 較正用基準物質
社内標準品
操作上の注意
操作上の注意
1. 測定試料の性質、採取法
- 検体として、EDTA 加血漿、ヘパリン加血漿又は血清を使用してください。
- 検体は凍結(-30°C)又は冷蔵(4°C)で21日間保存可能です。凍結検体を使用する場合は、20~30°C(目安)で融解し、よく混和してから使用してください。凍結融解を繰り返し行うことは避けてください。
- 濁りのある検体、肉眼で観察できる沈殿物のある検体は測定前に遠心分離を行い、使用してください。
2. 妨害物質・妨害薬剤
抱合ビリルビンは20.2mg/dL、非抱合ビリルビンは20.1mg/dL、ヘモグロビンは450mg/dL、乳びは1,770FTU、リウマチ因子は500IU/mL、トリグリセライドは2,000mg/dL、HAMAは1,000ng/mLまで影響は認められませんでした。
使用上又は取扱い上の注意
1. 取扱い上(危険防止)の注意
- 検体はHIV、HBV、HCV等の感染の恐れがあるものとして取り扱ってください。
- 感染の危険を避けるため、保護手袋、専用の実験衣を着用し、口によるピペッティングは行わないでください。
- 停止液は酸性溶液(0.5mol/L硫酸)です。使用に際しては、保護手袋、保護眼鏡等を着用し、液が皮膚についたり、目に入ったりしないように注意してください。
- 試薬が誤って目や口に入った場合は、水で十分洗い流す等の応急処置を行い、必要があれば医師の手当等を受けてください。
2. 使用上の注意
- 貯蔵方法に従って保存し、使用期限を過ぎた試薬は使用しないでください。使用期限は包装の表示をご確認ください。
- 反応時間及び反応温度は定められた条件で行ってください。また、操作開始後は、速やかに全操作を行い、各反応時間が一定となるように操作してください。
- 検体を測定するたびに、必ず検量線用標準液も同時に測定して検量線を作成してください。
- 一度他の容器に移した基質液は、戻さずに廃棄してください。また基質液は光に鋭敏な試薬です。発色反応中は必ず遮光し、青く着色した基質液は使用しないでください。
- 容器に破損が認められた場合は使用しないでください。
- 製造番号が異なる試薬を注ぎ足したり、組み合わせたりして使用しないでください。ただし、補充用として個別に販売する濃縮洗浄液については、その限りではありません。
- 洗浄が不十分な場合、ばらつきや偽陰性、偽陽性を生じることがありますので、十分に洗浄してください。
- クロスコンタミネーションを防ぐため、液の泡立ちや周囲への付着が起こらないようにしてください。
- 標識抗体液は酵素標識抗体を含有しています。各発色液への混入が起こらないように器具を分けて使用してください。
3. 廃棄上の注意
- 検体希釈液には0.02%のアジ化ナトリウムが含まれています。廃棄する際は爆発性の金属アジドが生成されないように大量の水とともに流してください。
- 試薬及び容器等を廃棄する場合は、廃棄物に関する規則に従って、医療廃棄物又は産業廃棄物等、区別して処理してください。
- 廃液の処理にあたっては、水質汚濁防止法などの規則に従ってください。
- 使用した器具(ピペット等)は次亜塩素酸ナトリウム(有効塩素濃度1,000ppm、1時間以上浸漬)、グルタールアルデヒド(2%、1時間以上浸漬)等による消毒処理又はオートクレーブ(121°C、20分以上)による滅菌処理を行ってください。
- 検体、廃液等が飛散した場合には次亜塩素酸ナトリウム(有効塩素濃度1,000ppm)、グルタールアルデヒド(2%)等によるふき取りと消毒を行ってくだい。
参考文献
- 自社データ